2024深圳国际体外诊断试剂展览会-组委会官网
Shenzhen International Examination Medical and IVD Exhibition 2024
Shenzhen International Examination Medical and IVD Exhibition 2024
深圳国际会展中心(宝安国际会展中心)

TGA(澳大利亚药品管理局)于近日发布通知称,自11月1日起,新冠抗原快速自测试剂盒可以供家庭自测使用。与所有其他新冠检测试剂盒一样,自测试剂需要TGA 批准并获得ARTG(澳大利亚医疗用品注册登记)。

此前,TGA已为这些试剂盒的潜在供应商开放了意向注册。因此,TGA目前正在开始受理自2021年11月1日起供应的新冠抗原快速自测试剂的ARTG注册申请。TGA 将审查所有申请并考虑在意向注册期间已提交的信息。

此前一周,我们曾发布了澳大利亚对于新冠抗原检测试剂的合法使用规定更新(点击回顾)。除了对于合法使用的规定更新之外,TGA还公布了《抗原快速自测的性能要求和降低风险策略指南》、《用于抗原快速自测的软件监管要求指南》,对新冠抗原自测试剂的准入提出了详细的要求和指引。
TGA在ARTG中提出了供应新冠抗原自测试剂的10项必须条件。这些强制性的条件涉及以下几个方向的内容:
用户支持服务
使用说明书
临床研究
投诉
上市后监管报告
西澳大利亚州和南澳大利亚州有各自当地的计划,可能并不会参与这项全国性的新冠抗原家庭自测试剂开放。
在TGA的官网上,我们还注意到,目前第一批拿到澳大利亚抗原家庭自测试剂准入的有多家中国企业。最早的入场企业是半个月前才拿到的批准,最晚的则是11月3号刚刚获批。

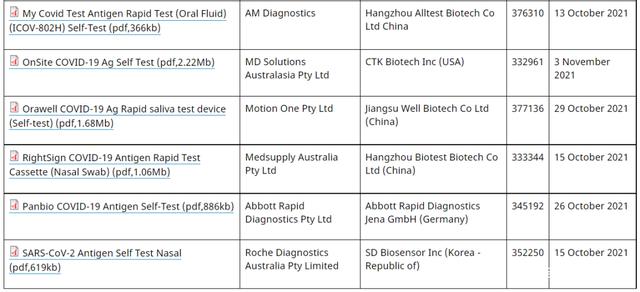
↑ TGA官网截图
现在提出申请还不晚!澳大利亚对于home test家用自测试剂的准入开放,才刚刚开始;对于想要进入澳大利亚IVD市场的国内企业来说,近期TGA的多项举措是一个强烈的信号。
通过澳方目前对于开放新冠家用自测试剂的大量需求;拿到ARTG,快速入场,第一时间抢占市场份额!